- рак молочной железы
у женщин (около 60 на 100000 человек в год, примерно 20% всех
опухолей, 3 место как причина смертности)
- рак предстательной
железы у мужчин (в США - 29% - 1 место, в России –
9.8 на 100000 человек в год – 9 место – 3,3% всех опухолей,
в Санкт-Петербурге – 7 место, 4 место как причина смертности).
- опухоли яичников
(10-15 на 100000 человек в год – 6,4% всех опухолей, 20% среди
опухолей женской половой сферы),
- матки (20
на 100000 человек в год, 6,8% среди всех опухолей, 3 место среди
заболеваний женских половых органов), а также (по мнению некоторых
авторов)
- рак поджелудочной железы
(10 на 100000, 2,7- 3,2% всех опухолей),
- яичек
(1-2% всех злокачественных опухолей) и
- щитовидной железы
(1% всех злокачественных заболеваний, 3 на 100000)
Совокупный удельный вес всех гормонозависимых
опухолей составляет 40-42%, что делает рассмотрение данной темы
весьма актуальным.
к оглавлению
Принципы и особенности гормональной
регуляции в норме и при патологии.
При разработке схем лечения опухолей гормонозависимой
сферы мы не можем не учитывать основные принципы и некоторые особенности
гормональной регуляции в норме и при патологии.
Итак:
1. Гормоны действуют на свои клетки-мишени, вызывая
в них соответствующие изменения. В нашем контексте важно знать,
какие гормоны вызывают усиленное деление клеток – мишеней и их
дифференциацию, а также
2. какие гормоны этому препятствуют. Соответственно,
постулируется функциональный агонизм – антагонизм гормонов.
3. Существует иерархия в системе гормональной
регуляции. На «самом верху» – гипоталамус, «ниже» - гипофиз. Оба
органа объединяются в гипоталамо-гипофизарную систему (ГГС). Гипоталамус
вырабатывает релизинг-факторы, действующие на гипофиз. Тот, в
свою очередь, продуцирует тропины, оказывающие влияние на нижележащее
звено – периферические эндокринные железы, которые секретируют
«окончательные» (если позволено будет так выразится) гормоны,
действующие на клетки мишени по всему организму.
Рассматривая всю цепочку «от верха до низа», имеющую преимущественное
отношение к той или иной сфере, выделяют так называемые оси. Например:
ГГС – яичники (или яички) – молочная железа, матка (или предстательная
железа) составляют половую ось. ГГС – щитовидная железа – это
тироидная ось.
В связи с этим важно понимать, что
4. промежуточные звенья – органы в каждой оси
являются одновременно и органом- мишенью для гормонов вышестоящего
регуляторного звена, и, наоборот, сами вырабатывают гормоны, имеющие
точку приложению на ниже расположенном звене. Таковы гипофиз,
яичники, яички.
5. наличие кибернетических механизмов межзвеньевого
взаимодействия, а именно отрицательной и положительной обратной
связи. Например, избыток эстрадиола в крови воспринимается гипоталамо-гипофизарной
системой как сигнал к понижению выработки половых тропинов.
6. некоторые опухоли эндокринных органов, в том
числе и гормонопродуцирующие опухоли, приобретают почти абсолютную
автономию и не реагируют на тормозящие влияния «сверху».
В качестве примера разберем ситуацию с опухолью
молочной железы.
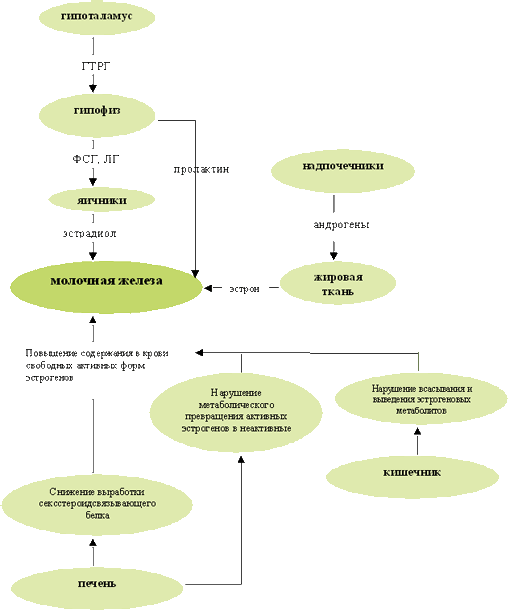
Основной провоцирующий гормон – эстрадиол (Е2) – вырабатывается
яичниками под действием фолликулостимулирующего гормона гипофиза
(ФСГ), который, в свою очередь, секретируется в ответ на гонадотропный
рилизинг – гормон (ГТРГ) гипоталамуса (см.
рис. 1).
Эта схема сохраняется для опухолей тела матки и эндометрия.
Для простаты схема аналогична, с той лишь разницей, что промежуточное
звено – яички, «окончательные» гормоны – андрогены, и, соответственно,
функциональные антагонисты – эстрогены и прогестагены.
Фармакологические принципы
Чем «ниже» расположен орган – мишень, тем больше
способов повлиять на процесс. Есть возможность: 1. блокировать
выработку тропинов гипофиза; 2. блокировать синтез гормонов в
периферической железе; 3. блокировать рецепторы к гормонам, находящиеся
на мембранах клеток органов-мишеней; 4. инактивировать гормоны
до их взаимодействия с рецептором.
Если же «подняться выше» по половой оси (см.
рис.1), и рассмотреть опухоли яичников, становится очевидным,
что из значимых направлений воздействия остается только блокада
выработки ГТРГ и гонадотропинов гипофиза.
Это можно осуществить за счет 1) агонистов ГТРГ; 2) ингибиторов
гипофизарной секреции, 3) веществ, связывающих гормоны.
Кроме того, имеется теоретическая возможность воздействовать на
процесс через отрицательную обратную связь. Однако по понятной
причине данный принцип не применим при опухолях половой сферы.
Противоопухолевое лечение с вовлечением механизма отрицательной
обратной связи хорошо работает при опухолях щитовидной железы,
и имеет вид так называемой супрессивной терапии. Для этого назначаются
гормоны щитовидной железы (и подобные им вещества из растений)
в дозе, настолько великой, чтобы подавить выработку ТТГ. К слову,
в пересчете на тироксин эта доза составляет 150 мкг в сутки.
Нужно отметить, что точки воздействия на систему гормональной
регуляции при назначении противоопухолевого лечения могут комбинироваться
в составе единой лечебной схемы. Например, при неоперабельном
раке предстательной железы одновременно назначают агонист ГТРГ
и блокатор андрогеновых рецепторов.
Исходя из вышесказанного, нетрудно представить себе фармакологические
принципы лечения гормонозависимых опухолей:
1. Использование функциональных антагонистов гормонов.
О функциональном антагонизме между гормонами (подобными им веществами,
например, из растений) можно говорить тогда, когда в своем действии
на орган-мишень, они вызывают противоположные по смыслу эффекты.
При этом точки приложения на мембране клетки (клеточный рецептор)
разные.
Например, функциональными антагонистами являются эстрогены и андрогены,
что позволяет первые применять для лечения рака предстательной
железы, а вторые – рака молочной железы. Исторически, этот подход,
вероятно, самый старый, что связано с хронологией синтеза гормональных
препаратов. Применение эстрогенов при раке простаты продолжает
иметь место, андрогены же при заболеваниях молочных желез уже
не используются из-за низкой эффективности и выраженных побочных
эффектов.
Пример из траволечения: назначение растений, содержащих фитоэстрогены,
для лечения рака предстательной железы – дягиль, клевер, люцерна
и т.п.
2. Использование агонистов рецепторов с минимальной
функциональной активностью, но обладающих высоким сродством к
гормональным рецепторам. В отличие от предыдущих средств, лечебное
вещество действует на тот же рецептор, что и гормон.
Пример из классики лечения опухолей молочных желез – тамоксифен
(зитазониум, нолвадекс). Препарат, специфически связываясь с рецептором
к эстрогену, не позволяет последнему воздействовать на клетку
и осуществлять свои стимулирующие функции. Однако, как оказалось,
тамоксифен не является в чистом виде блокатором эстрогенового
рецептора, но и сам обладает легким стимулирующим эффектом. Такое
положение вещей вполне удовлетворяет целям лечения, так как нивелируются
побочные эффекты от полной блокады эстрогеновых рецепторов (остеопороз,
артериальная гипертония). Отрадно отметить, что исследования последних
лет, касающиеся эффектов некоторых биофлавоноидов, по сути являющихся
фитоэстрогенами, подтвердили актуальность последних для профилактики
и лечения опухолей молочной железы, эндометрия и простаты. Таковым,
например, является генистеин сои, у которого сродство
по отношению к рецептору эстрадиола составляет всего 5%. В последние
годы огромное внимание уделяется научному изучения многих известных
фитоэстрогенов (формононетин, наригенин, дайдзеин, эквол, хризин
и др.).
3. Использование средств, выключающих центральную
стимуляцию.
Чаще всего воздействие, основанное на данном принципе, осуществляется
на гипофиз. В частности, очень интересным выглядит методика с
применением агонистов рецепторов к ГТРГ (бусерелин, гезерелин
и т.п.). В отличие от средств, описанных в предыдущем пункте,
стимулирующий эффект агонистов ГТРГ не уступает естественному
гормону.
Известно, что гипоталамус вырабатывает ГТРГ в импульсном режиме.
Если агонист рецептора ГТРГ назначать в таком же импульсном режиме,
то можно получить стимуляцию выработки половых тропинов гипофиза
(что и используется при некоторых эндокринных болезнях, например,
при гипофизарном гипогонадизме).
В случае с опухолями агонисты ГТРГ назначают в постоянном режиме,
после легкой кратковременной стимуляции, наступает угнетение выработки
гипофизом ФСГ и ЛГ.
В расчете на подобный эффект в фитотерапии могут быть назначены
прострел луговой, полынь обыкновенная и некоторые другие растения.
Данная позиция пока скорее теоретическая, и требует обоснования
и отработки доз и режима применения на экспериментальных моделях.
Весьма благодатную почву для размышлений в направлении воздействия
на гипофиз представляют народные методы контрацепции. Так, например,
известно, что длительный прием отваров зюзника европейского и
воробейника краснокорневого делает невозможным наступление беременности
у некоторых женщин.
В результате многочисленных экспериментов было установлено, что
контрацептивный эффект указанных растений связан с угнетением
ими гонадотропной функции гипофиза. Достоверно известно, что активным
началом этих растений является литоспермовая кислота и шиконин.
Данная информация позволяет сделать вывод, который находит экспериментальное
подтверждение, что растения, содержащие указанные вещества, обладают
антигонадотропным эффектом и, соответственно, могут использоваться
в лечении гормонозависимых опухолей.
Литоспермовую кислоту содержат многочисленные представители семейства
Boraginacea, давно и прочно вошедшие в рецептуру народной медицины:
окопник лекарственный, чернокорень лекарственный, воловик
(анхуза), синяк обыкновенный.
Нужно отметить, что литоспермовая кислота и шиконин, помимо антигормонального
эффекта, обладают также некоторым прямым противоопухолевым действием,
механизмы которого активно изучаются в последние годы.
Например, известно, что шиконин может блокировать теломеразу,
участвующую в процессе клеточного деления. Кроме того, он индуцирует
апоптоз и блокирует рецепторы к тканевым факторам роста, расположенные
на мембранах опухолевых клеток.
Имеется ряд экспериментальных данных, а также наши собственные
наблюдения, которые показывают, что и зюзник, и воробейник
способны понижать выработку гипофизом тиреотропного гормона,
что вполне может использоваться и используется нами в качестве
супрессивной терапии при раке щитовидной железы.
Механизм действия литоспермовой кислоты на гипофиз распознан не
окончательно. Наиболее вероятно специфическое влияние вещества
на какие-то рецепторы на мембранах гонадотрофов, препятствующее
адекватной реакции на ГТРГ. Данный факт требует отнести бурачниковые
к категории средств, угнетающих гипофизарную секрецию и, естественно,
отличает их от агонистов ГТРГ.
Возвращаясь к теме агонистов в области центрального звена регуляции,
нельзя не вспомнить агонисты дофаминовых рецепторов. Благодаря
дофаминовому контролю сохраняется на постоянном уровне пролактин.
Поэтому когда возникают какие-либо нарушения выработки этого нейромедиатора
в гипоталамусе или затруднения его пассажа по ножке гипофиза,
уровень пролактина начинает расти, нередко достигает внушительных
цифр.
Роль пролактина в возникновении и прогрессировании опухолей молочной
и предстательной железы изучена довольно хорошо.
При назначении лечебных схем в отношении рака данных локализаций,
сейчас обычно ограничиваются блокадой эстрогенов и андрогенов
соответственно. Считается, что этого достаточно. Однако данные
по лечению больных раком молочной железы с метастазами в кости,
направленное на понижение уровня сывороточного пролактина, убедительно
доказывают положительный эффект такого мероприятия.
Классический пример дофаминового агониста – бромокриптин – напоминает
по своей структуре некоторые алкалоиды спорыньи, которая
с давних времен использовалась для лечения различных диэнцефальных
расстройств.
Классическими также можно считать сочетания вытяжек из спорыньи
и извлечений из растений семейства пасленовых - красавки,
дурмана и белены. Нетрудно заметить, что все перечисленные
растения являются ядовитыми. В связи с этим их использование в
качестве фитотерапевтических средств ограничено.
Перспективно в рассматриваемом контексте применение прутняка,
клопогона даурского, лукосемянника даурского, воронца кустарникового,
кирказона ломоносовидного, боярышника кровавокрасного и некоторых
других растений.
4. Использование средств, непосредственно угнетающих
функцию эндокринных органов, вырабатывающих «конечные» гормоны.
Так, например, известно, что хлопчатник (госсипол) угнетает
функцию яичек, а корни кубышки желтой, трава проломника северного
аналогичным образом действуют на яичники.
Применение данных лекарств имеет ряд недостатков. Так, в частности,
хлопчатник не столько угнетает гормональную активность яичек,
сколько обладает сперматоцидным действием. Угнетение сперматогенеза,
связанное с повреждением эпителия извитых канальцев яичек, нередко
приобретает необратимый характер и в 26% случаев заканчивается
бесплодием.
5. Использование средств, влияющих на различные
ферментные системы, участвующие в синтезе и метаболизме гормонов,
как в железах, так и экстрагландулярно.
Так, вещества, содержащиеся в красном винограде (ресвератрол),
а также хризин и нарингенин, выделенные из других растений, могут
блокировать фермент ароматазу, превращающий тестостерон в эстрадиол,
а также дигидроэпиандростерон в эстрон. Интересно, что дайдзеин
и генистеин (соевые флавоноиды) в отношении человеческой рекомбинантной
ароматазы неактивны. Мало того, в эксперименте было показано,
что генистеин в дозах от 1 nM до 1 mM может стимулировать ароматазу
стромальных клеток эндометрия. Высказывается мнение, что генистеин
усиливает экспрессию гена, ответственного за синтез ароматазы.
Далее, ресвератрол обладает способностью конкурентно связываться
с андростендионом, не позволяя ему вступить в ароматизацию.
Генистеин дрока красильного и сои стимулирует выработку
печенью эстрогенсвязывающего протеина, белка, специфически соединяющегося
в крови с эстрогенами, в результате чего они становятся неактивными.
Кроме того, он тормозит выработку веществ (фактор Боумена-Берка
– ингибитор опухолевых протеаз), которые отвечают за опухолевый
неоангиогенез (образование новых сосудов в опухоли).
Специфические соединения серы, входящие в состав семейства крестоцветных
(различные сорта капусты, сурепка, ярутка полевая, горчица
и т.п.) – изотиоцианаты и глюкозоиналаты (в частности, индол –
3 - карбинол) – переводят активные метаболиты эстрогенов в неактивные,
выполняя функцию одной из ферментных систем.
Вещества, содержащиеся в лилии широколиственной, сереное пильчатой
(сабаль), блокируют 5 – альфа – редуктазу, переводящую тестостерон
в дигидротестостерон.
6. Вспомогательные средства, влияющие на утилизацию
гормонов в печени, всасывание в кишечнике, выведение со стулом
и прочие аспекты метаболизма.
Классификация растений
Таким образом, анализируя уже известные и предполагаемые
механизмы действия растений на различные звенья эндокринной регуляции,
в том числе и при лечении гормонозависимых опухолей, можно представить
себе следующую классификацию:
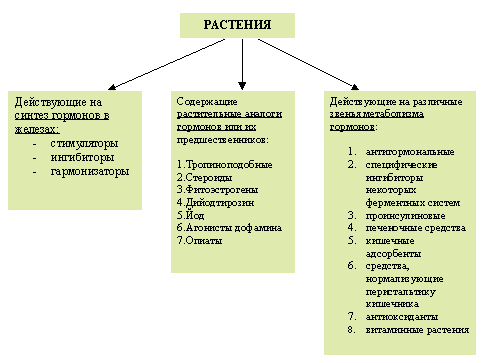
Такое подразделение растений имеет практическую
ценность, заключающуюся в упрощении подбора трав в состав простого
сбора и для составления сложного многокомпонентного курса лечения
различных гормонозависимых опухолей.
Гормонорегуляторный блок
Траволечение онкологического больного, в том числе
и больного гормонозависимым вариантом опухоли, - задача, далеко
не исчерпывающаяся коррекцией гормонального фона. Поэтому можно
говорить о формировании «гормонорегуляторного блока» (ГРБ) в составе
сложного травяного курса:
- Гормонорегуляторный блок -
одно или несколько растений, объединенных по принципу целенаправленного
влияния на гормональную сферу, входящие в состав целостной травяной
схемы лечения онкологического больного.
Излишне говорить, что выбор растений для ГРБ основывается
на предполагаемом патогенезе гормонозависимой опухоли в каждом
конкретном случае.
В качестве демонстрации возьмем следующий виртуальный пример.
Больная М., 36 лет. Диагноз: Рак молочной железы.
Менструальный цикл сохранен.
Задачи, которые
должен решать в данной ситуации ГРБ: |
Вариант
растения |
Используемая
часть |
Уменьшить стимуляцию яичников гонадотропинами гипофиза
(понизить выработку ФСГ гипофизом)
|
Воробейник лекарственный
|
трава |
Блокировать синтез эстрогенов непосредственно в яичниках
|
Кубышка
желтая |
корень |
Блокировать
рецепторы к эстрогенам, расположенные на клетках опухоли |
Дрок красильный
|
трава |
Оптимизировать
работу печени по ферментативной утилизации эстрогенов
и синтезу сексстероидсвязывающего белка |
Бессмертник песчаный
|
соцветия |
Наладить внутрикишечное
связывание и выведение эстрогеновых метаболитов. |
Алтей
лекарственный |
корень |
Контроль эффективности
гормонально ориентированного травяного лечения осуществляется
традиционными методами, а именно определением уровней гормонов,
в отношении которых проводится воздействие (ФСГ, ЛГ, ТТГ, эстрадиол,
тестостерон).
В заключение остается добавить, что мягкое, практически лишенное
побочных реакций действие трав позволяет проводить лечение различных
предопухолевых состояний, таких как доброкачественная гиперплазия
предстательной железы, различные формы мастопатии, миома матки,
эндометриоз, доброкачественный узловой зоб.
к оглавлению
Рис. №1. Схема гормональной регуляции молочной
железы в норме и при патологии.
к оглавлению
|


